Alam semesta terdiri atas planet-planet, contohnya bumi. Di bumi terdapat gunung, udara, laut, dan begitu banyak hal lain. Segala sesuatu yang berada di bumi tersusun atas materi, yang terdiri atas unsur, seperti air, udara, tanah, dan api. Itulah gambaran keragaman materi.
Klasifikasi Materi
Para ilmuwan mengklasifikasi materi agar lebih mudah dipelajari dan disusun secara sistematis. Materi adalah sesuatu yang mempunyai massa dan dapat menempati sebuah ruang. Materi berdasarkan wujudnya dapat dikelompokkan menjadi zat padat, cair, dan gas. Contoh zat padat adalah beberapa jenis logam, seperti besi, emas, dan seng. Air, minyak goreng, dan bensin merupakan contoh wujud cair. Contoh zat berwujud gas adalah udara, asap, dan uap air.
Contoh wujud zat yang sederhana dan mudah kamu pahami adalah air. Ketika dalam bentuk bongkahan es, maka es tersebut dikatakan dalam wujud padat. Tetapi, ketika dipanaskan es tersebut akan berubah kembali menjadi air. Air tersebut dikatakan dalam wujud cair. Ketika dipanaskan pada suhu 100°C, air akan berubah menjadi uap air. Uap air dikatakan dalam wujud gas. Perbedaan sifat zat padat, cair, dan gas dijelaskan pada Tabel berikut ini.
| Padat | Cair | Gas |
| Mempunyai bentuk dan volume tertentu. | Mempunyai volume tertentu, tetapi tidak mempunyai bentuk yang tetap, bergantung pada media yang digunakan. | Tidak mempunyai volume dan bentuk yang tertentu. |
| Jarak antarpartikel zat padat sangat rapat. | Jarak antarpartikel zat padat sangat rapat. | Jarak antarpartikel gas sangat renggang. |
| Partikel-pertikel zat padat tidak dapat bergerak bebas. | Partikel-pertikel zat cair dapat bergerak bebas, namun terbatas. | Partikel-partikel gas dapat bergerak sangat bebas. |
Unsur, Senyawa, dan Campuran
Unsur
Semua benda yang ada di bumi kita tersusun dari materi. Ilmuwan menggolongkan materi berdasarkan komposisi dan sifatnya. Berdasarkan komposisinya, materi yang ada di alam dapat diklasifikasi menjadi zat tunggal dan campuran.
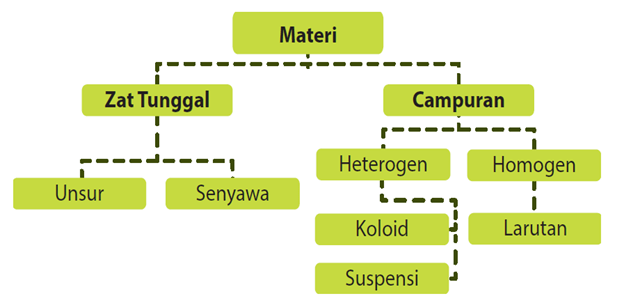
Materi di alam dapat dibagi menjadi zat murni dan campuran. Zat tunggal (murni) yang ada di alam dapat dibagi menjadi unsur dan senyawa. Unsur merupakan zat tunggal yang tidak dapat dibagi lagi menjadi bagian yang lebih sederhana dan akan tetap mempertahankan karakteristik asli dari unsur tersebut. Sebongkah emas apabila dibagi terus sampai bagian yang terkecil akan menjadi atom emas. Bagian terkecil dari unsur adalah atom.
Para ahi kimia menggunakan simbol atau lambang untuk menunjukkan perbedaan antara unsur kimia yang satu dengan yang lainnya. Ahli kimia sudah menemukan unsur sejak abad ke-9 dan unsur secara bertahap terus berkembang sampai abad ke-20. Unsur di alam dapat dibagi menjadi dua jenis, yaitu unsur logam dan nonlogam.
Contoh unsur nonlogam dan lambangnya
| Nama Latin | Nama Indonesia | Lambang |
| Aluminium | Aluminium | Al |
| Aurum | Emas | Au |
| Argentum | Perak | Ag |
| Cuprum | Tembaga | Cu |
| Ferrum | Besi | Fe |
Contoh unsur logam dan lambangnya
| Nama Latin | Nama Indonesia | Lambang |
| Oxygen | Oksigen | O |
| Hydrogen | Hidrogen | H |
| Carbon | Karbon | C |
| Sulphur | Belerang | S |
| Phosphorus | Fosfor | P |
Unsur diberi nama dengan menggunakan bahasa Latin berdasarkan penemu pertamanya atau tempat ditemukannya unsur tersebut. Ahli-ahli kimia tidak membedakan penamaan unsur alamiah yang terdapat di alam ataupun unsur buatan.
Simbol unsur dibuat untuk memudahkan dalam penulisan nama unsur, yaitu dengan cara menyingkatnya. Simbol unsur yang saat ini digunakan secara internasional adalah simbol unsur yang diusulkan oleh Jöns Jacob Berzelius. Cara pemberian lambang unsur menurut Berzelius adalah sebagai berikut:
- Setiap unsur dilambangkan dengan satu huruf, yaitu huruf awal dari nama latinnya.
- Huruf awal ditulis dengan huruf kapital atau huruf besar.
- Untuk unsur yang memiliki huruf awal sama, diberikan satu huruf kecil dari nama unsur tersebut.
Contoh:
Karbon (nama latinnya Carbon), dilambangkan dengan (C), Kalsium (nama latinnya Calsium) dilambangkan dengan (Ca).
Unsur-unsur tersebut selanjutnya disusun dalam bentuk sistem periodik unsur. Unsur-unsur yang memiliki sifat yang hampir sama diletakkan dalam satu kolom. Unsur-unsur logam terletak di bagian kiri bawah (diberi simbol warna biru), unsur-unsur nonlogam terletak di bagian kanan atas (diberi simbol warna kuning), sedangkan unsur semilogam (diberi warna cokelat) di antara warna biru dan kuning.
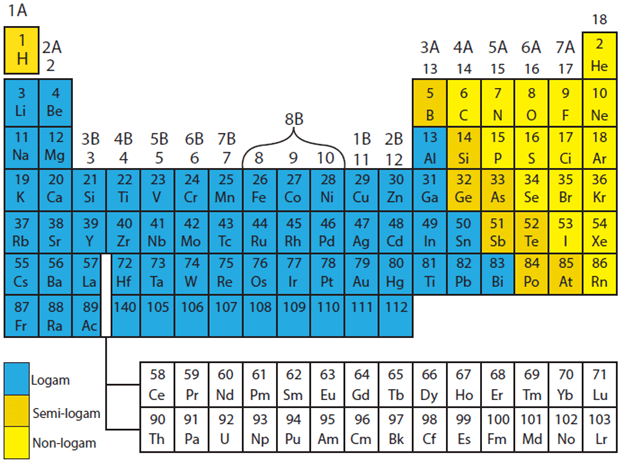
Unsur logam dan nonlogam memiliki perbedaan sifat fisika dan kimia. Berikut perbedaan sifat unsur logam dan nonlogam.
| Logam | Nonlogam |
| Berwujud padat pada suhu kamar (kecuali raksa).Dapat ditempa dan dapat diregangkan.Konduktor listrik dan panas. | Ada yang berwujud padat, cair, dan gas.Bersifat rapuh dan tidak dapat ditempa.Nonkonduktor, kecuali grafit. |
Senyawa
Kita sering menggunakan air, gula, garam, asam cuka, dan beberapa bahan lainnya. Bahan-bahan tersebut merupakan senyawa. Bagian terkecil dari sebuah unsur adalah atom. Dua atau lebih atom dapat bergabung melalui reaksi kimia dan membentuk molekul. Molekul merupakan bagian terkecil dari suatu senyawa. Jadi, senyawa terdiri atas dua buah unsur atau lebih. Suatu senyawa masih dapat diuraikan menjadi unsur-unsurnya.
Senyawa merupakan zat tunggal/murni yang dapat diuraikan menjadi dua atau lebih zat yang lebih sederhana dengan proses kimia biasa. Misalnya, air yang memiliki rumus H2O dapat diuraikan menjadi unsur hidrogen (H) dan oksigen (O).
Senyawa terbentuk melalui proses pencampuran unsur secara kimia. Sifat suatu senyawa akan berbeda dengan sifat unsur-unsur penyusunnya. Misalnya, sifat air sebagai senyawa akan berbeda dengan sifat gas hidrogen dan oksigen sebagai unsur penyusunnya.
Campuran
Beberapa campuran yang sering kita jumpai dalam kehidupan sehari-hari misalnya susu cokelat, air sungai, udara, batuan, garam beryodium, paduan, teh manis atau kopi. Campuran adalah suatu materi yang terdiri atas dua zat atau lebih yang masih mempunyai sifat zat asalnya. Campuran dibedakan menjadi dua, yaitu campuran homogen dan campuran heterogen.
1) Campuran Homogen
Larutan gula, larutan garam, dan sirop merupakan contoh campuran homogen. Campuran homogen adalah campuran yang tidak dapat dibedakan zat- zat yang tercampur di dalamnya.
Larutan tersusun atas pelarut (solvent) dan zat terlarut (solute). Pelarut yang banyak digunakan adalah air. Senyawa lain yang dapat digunakan sebagai pelarut adalah senyawa organik yang dikenal juga sebagai pelarut organik, contohnya kloroform dan alkohol.
Dalam larutan, ukuran partikel zat terlarut sangat kecil dengan diameter kurang dari 1 nm sehingga partikel zat terlarut tidak dapat dilihat walaupun menggunakan mikroskop ultra. Oleh karena itu, larutan terlihat homogen (serba sama). Artinya zat yang terlarut dan pelarut dalam larutan tersebut tidak dapat dibedakan.
Larutan Asam. Ciri-cirinya adalah:
- Rasanya masam (tidak boleh dicoba kecuali dalam makanan).
- Dapat menimbulkan korosi.
- Mengubah kertas lakmus biru menjadi merah.
Larutan Basa. Ciri-cirinya adalah:
- Mempunyai rasa agak pahit (tidak boleh dicoba).
- Terasa licin di kulit.
- Mengubah kertas lakmus merah menjadi biru.
2) Campuran Heterogen
Campuran pasir dan air merupakan salah satu contoh dari campuran heterogen. Campuran heterogen terjadi karena zat yang tidak dapat bercampur satu dengan lain secara sempurna sehingga dapat dikenali zat penyusunnya. Pada campuran heterogen, seluruh bagiannya tidak memiliki komposisi yang sama (tidak serba sama).
Perbedaan sifat unsur, senyawa, dan campuran
| Unsur | Senyawa | Campuran |
| Zat tunggalTidak dapat diuraikanTerdiri atas satu jenis atom | Zat tunggalDapat diuraikanTersusun atas dua jenis atom atau lebihPerbandingan massa zat penyusunnya tetap | CampuranDapat diuraikanTersusun atas dua jenis atom/molekul atau lebihPerbandingan massa zat penyusunnya tidak tetap |
Cara Memisahkan Campuran
Untuk memperoleh zat murni, penyusun campuran harus dipisahkan. Zat-zat dalam campuran tersebut dapat dipisahkan secara fisika. Prinsip pemisahan campuran didasarkan pada perbedaan sifat-sifat fisis zat penyusunnya, seperti wujud zat, ukuran partikel, titik leleh, titik didih, sifat magnetik, kelarutan, dan lain sebagainya.
Metode pemisahan campuran banyak digunakan dalam kehidupan sehari-hari seperti untuk penjernihan air dan pembuatan garam. Beberapa metode pemisahan campuran yang sering digunakan antara lain penyaringan (filtrasi), sentrifugasi, sublimasi, kromatografi, dan distilasi.
Filtrasi (Penyaringan)
Penyaringan adalah metode pemisahan campuran yang digunakan untuk memisahkan cairan dan padatan yang tidak larut berdasarkan pada perbedaan ukuran partikel zat-zat yang bercampur.
Sentrifugasi
Metode ini sering dilakukan sebagai pengganti filtrasi jika partikel padatan yang terdapat dalam campuran memiliki ukuran sangat halus dan jumlah campurannya lebih sedikit. Metode sentrifugasi digunakan secara luas untuk memisahkan sel-sel darah merah dan sel-sel darah putih dari plasma darah. Dalam hal ini, padatan adalah sel-sel darah merah dan sel-sel darah putih yang akan mengumpul di dasar tabung reaksi, sedangkan plasma darah berupa cairan yang berada di bagian atas.
Distilasi (Penyulingan)
Pemisahan campuran dengan cara penyulingan digunakan untuk memisahkan suatu zat cair dari campurannya. Prinsip kerjanya didasarkan pada perbedaan titik didih dari zat cair yang bercampur, sehingga saat menguap setiap zat akan terpisah.
Kromatografi
Kromatografi merupakan metode pemisahan campuran yangdidasarkan pada perbedaan kecepatan merambat antara partikel-partikel yang bercampur dalam suatu medium diam ketika dialiri suatu medium gerak. Jenis kromatografi yang paling banyak digunakan adalah kromatografi kertas. Jenis kromatografi lain adalah kromatografi lapis tipis dan kromatografi gas.
Sublimasi
Prinsip kerja metode pemisahan campuran dengan cara sublimasi didasarkan pada campuran zat yang memiliki satu zat yang dapat menyublim (perubahan wujud padat ke wujud gas) sedangkan zat yang lainnya tidak dapat menyublim. Contohnya, campuran iodin dengan garam dapat dipisahkan dengan cara sublimasi
